生物制药工业主要采用中国仓鼠卵巢(CHO)细胞生产稳定的单克隆抗体(mAbs),虽然连续操作工艺已经成功地应用于化学工业,但生物制药工业的主流仍然是Fed-batch的培养方式,而不是连续或灌注式培养。
传统的Fed-batch培养方式接种活细胞密度(VCD)约为0.5E6vc/ml。通过种子培养阶段(N-1阶段)引入灌流培养或工艺强化,将Fed-batch生产阶段(N阶段)中的接种密度提高到2-10E6 vc/ml,缩短培养生产时间并提高抗体产量。
本文研究表明,在同样的14天时间内,提高接种密度可以显著提高3个CHO GS细胞系生产的3种抗体的产量。研究证实在N-1步骤中使用Fed-batch的方法或使用富集培养基的非灌流方法同样可以获得22-34E6 vc/ml的高密度。将非灌流培养的N-1高密度种子接种到N阶段的生物反应器中,其接种VCD可达3-6E6 vc/ml,采用上述方式取得的抗体产量和质量属性与使用灌流式N-1种子接种的生物反应器相当。为了在N-1阶段获得高密度,基础培养基的富集在N-1阶段和随后的Fed-batch生产阶段中至关重要。与需要灌流设备的灌流N-1培养方式相比,非灌流N-1方法在操作上要简单得多,可用于工艺开发、工艺表征和大规模商业生产。
强化接种密度可提高Fed-batch生产培养的抗体产量
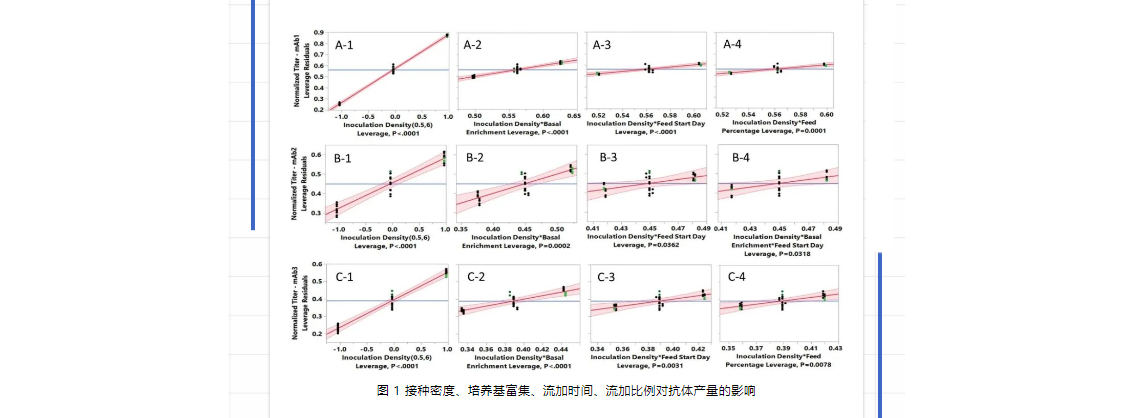
为了研究不同的接种密度和其他相关的细胞培养参数对最终产量的影响,首先在96个50ml的TubeSpin中对采用3个不同CHO K1 GS细胞系表达的3个抗体进行Fed-batch细胞培养评估。在TubeSpin培养中,筛选的因素是接种密度、基础培养基的富集程度、第一次添加补料的时间,以及每天的补料量占初始工作容积的百分比。如细胞系A(图1:A-1)、细胞系B(图1:B-1)和细胞系C(图1:C-1)的杠杆图所示,接种密度对提高3个细胞系的最终产量贡献最大。在最佳条件下,当接种密度由0.5E6 vc/ml增加到6E6 vc/ml时,细胞系A的滴度增加了3倍多。在较高的接种条件下,细胞系B和C也有类似的反应,Titer分别增加1.7倍和2.3倍。结论得出提高接种密度,从传统的0.5E6 到6E6 vc/ml,显著提高了3个抗体的最终产量。
采用非灌流式CHO种子培养获得更高的最高细胞密度
高接种密度的Fed-batch生产培养,在N-1种子培养阶段需要明显更多的细胞数量。为了评估N-1种子培养的非灌流方法是否能获得足够高的VCD,将3种非灌流N-1种子培养策略,即常规Batch、富集Batch和Fed-batch与灌流N-1培养进行了比较(图2和表1)。
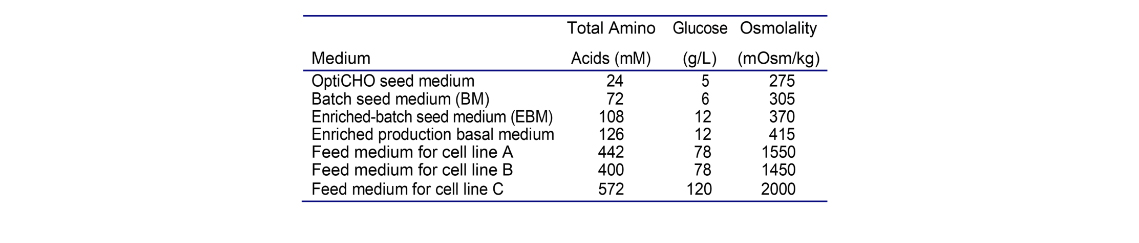
第一个实验考察了3个CHO K1 GS细胞系(接种密度:2E6 vc/ml)在Batch模式下使用3种不同的Batch培养基的N-1种子培养生长概况(图2和表1)。这3种种子培养基是OptiCHO、种子培养基(BM)和富集种子培养基(EBM)(表2)。如表2所示,相对的营养水平,以及渗透压的增加顺序为OptiCHO < BM < EBM。Batch培养种子的VCD峰值是按照OptiCHO、BM和EBM的顺序增加的(表2)。所有使用OptiCHO培养基的细胞系的VCD都明显较低(6-13 E6 vc/ml),第6天的存活率下降到73-86%(图2B,D,F)。BM种子条件下的生长达到了15-26E6 vc/ml的峰值VCD,但从第5-7天开始,细胞系A的VCD(图2A)和细胞活力(图2B)明显下降,从第4-6天开始,细胞系B和C的VCD(图2C-2F)明显下降。这种VCD和存活率的快速下降在生产中构成了风险。最好的结果是EBM的Batch培养,在6-7天的培养过程中达到了23-32E6 vc/ml的峰值VCD和高活力(图2和表1)。因此,EBM条件被选为N-1培养基条件。应该注意的是,过多的培养基富集可能导致N-1种子培养物中的CHO细胞生长受到抑制(数据未显示),这是因为较高的渗透压、较高浓度的葡萄糖或其他不明的抑制因素而引发的。
这3个细胞系还在Fed-batch和灌流培养中进行了评估(表1和图2)。细胞系A的Fed-batch种子培养取得了22E6 vc/ml的峰值VCD,这与EBM Batch培养条件相似(图2A)。细胞系B和C的Fed-batch种子培养的峰值VCD分别为32E6 和34E6 vc/ml(图2C,E),都略高于EBM Batch培养条件。此外,所有3个细胞系在Fed-batch模式下的种子培养的存活率都非常好,保持在99%左右(图2)。众所周知,灌流式N-1培养能使细胞保持在指数增长阶段,并能获得高的VCD。正如预期的那样,灌流式N-1培养物取得了明显较高的VCD,分别为44E6,41E6 和62 E6 vc/ml,细胞系A、B和C在第5天的存活率皆为99%(图2和表1)。

非灌流式N-1种子可用于接种强化Fed-batch生产
非灌流式N-1种子培养获得了高VCD和好的存活率之后,接下来评估这些N-1种子在强化的Fed-batch生产中的表现。
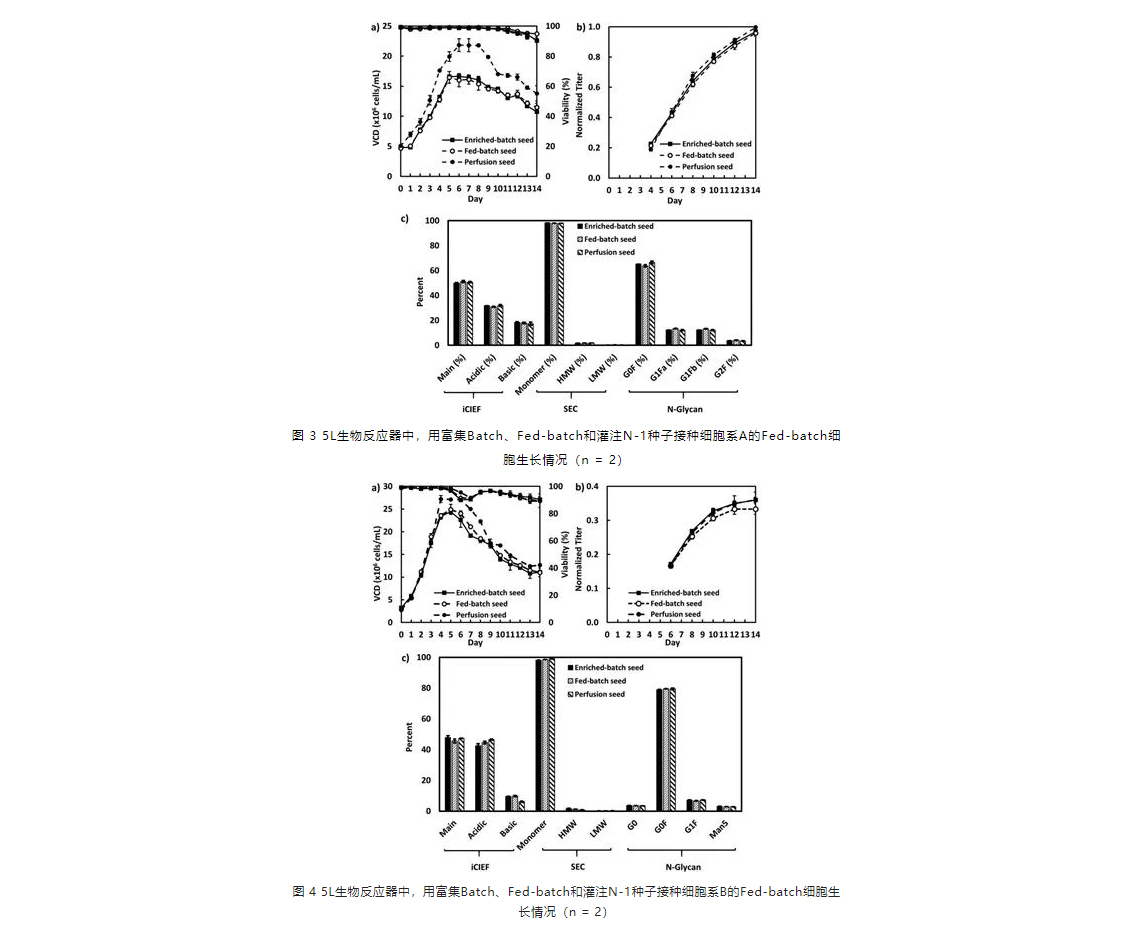
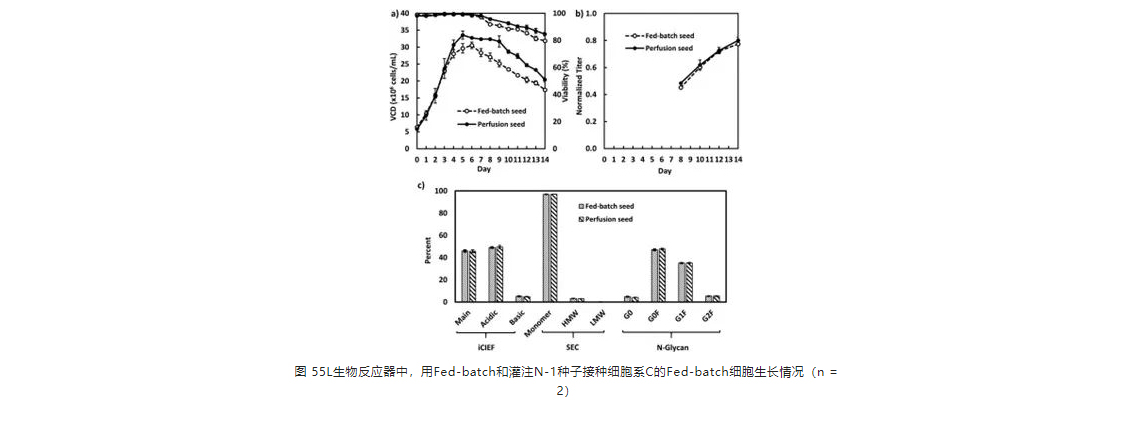
对于细胞系A N阶段Fed-batch培养是用同样的接种密度5E6 vc/ml(图3A[朱光凯1] )接种不同培养方式的种子。接种灌流N-1种子的生产培养物达到了最高的细胞密度,为22E6 vc/ml,而接种富集Batch或Fed-batch N-1种子的N阶段VCD峰值为17E6 vc/ml(图3A)。然而,所有培养物最终产量是相似的,从0.96 -1.00(图3B)。因此,虽然灌流N-1种子条件下取得了更高的VCD峰值,但这并没有导致这些培养物的最终产量显著增加。最重要的是,无论N-1种子如何操作,产品质量属性,包括电荷变体、SEC杂质和N-聚糖概况,对所有Fed-batch产物都是相似的(图3C)。对于细胞系B,使用第5天的N-1种子在富集Batch、Fed-batch和灌流模式下培养的种子分别以3E6 vc/ml的密度进行接种(图4)。与细胞系A类似,使用灌流式N-1种子接种的Fed-batch培养取得了最高的VCD峰值,但同样,在不同N-1条件下,抗体产量都是相似的,即0.33-0.36(图4B)。对于细胞系C,以6E6 vc/ml的密度接种,使用来自Fed-batch或灌流模式的第5天N-1种子进行培养(图5)。同样,两种生产培养物达到出相似的抗体产量和质量属性。
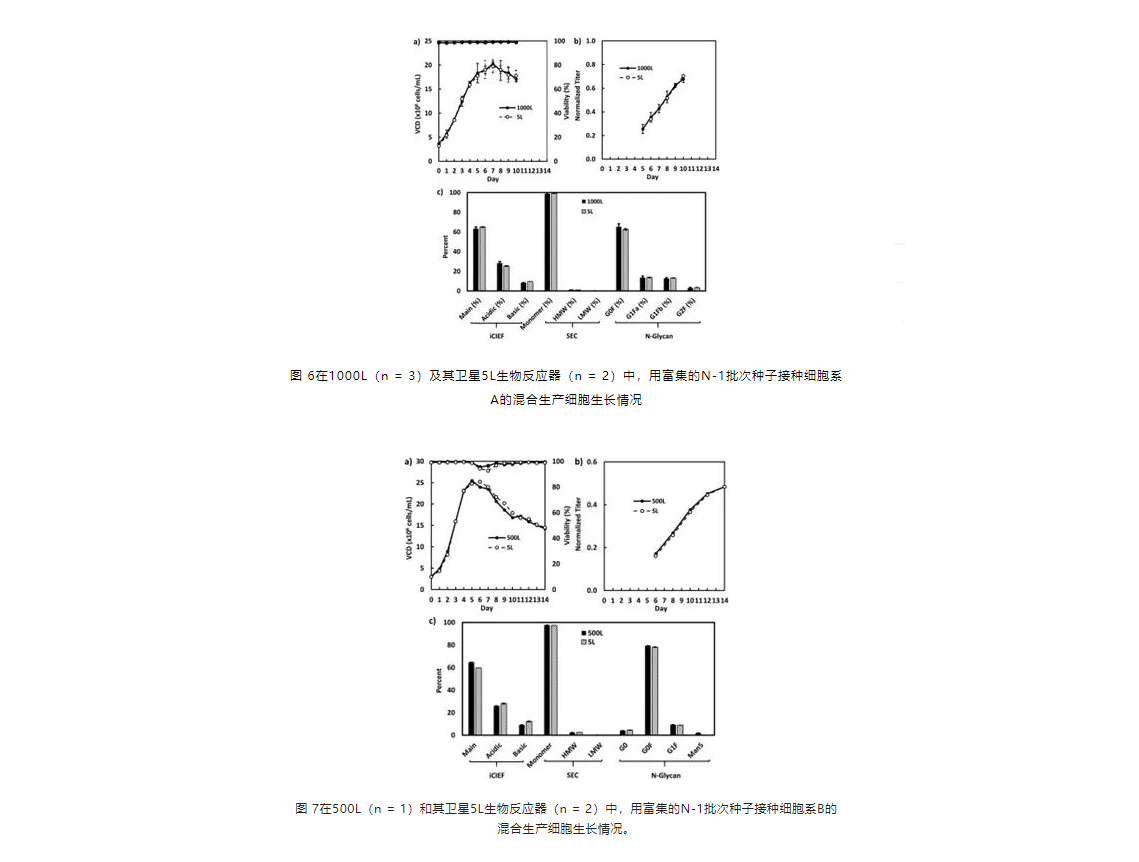
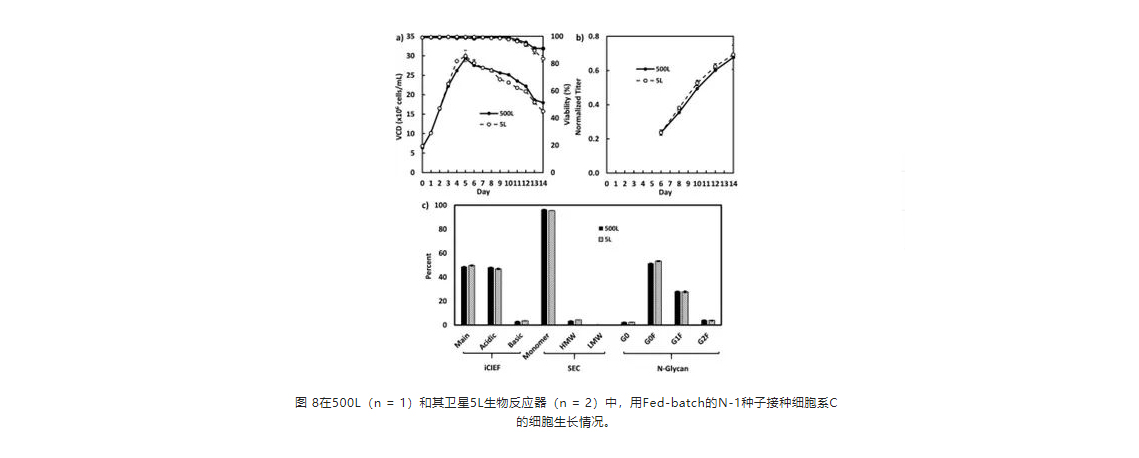
使用非灌流式N-1种子强化的Fed-batch工艺可以在500升或1000升的生物反应器中放大培养
细胞系A和B的富集batch N-1种子分别用于接种1000L(图6)和500L生物反应器(图7)中的强化Fed-batch生产培养,而细胞系C的Fed-batch的N-1种子则用于接种500L生物反应器中的强化Fed-batch生产培养(图8)。所有3个细胞系培养过程都被证明在500L或1000L生物反应器中是可扩展的。细胞密度、抗体产量和产品质量概况与5L生物反应器中的一致(图6-8)。
讨论
生产用基础培养基的富集与高接种量VCD有协同作用,高接种密度的Fed-batch培养可提高所有3种不同mAb的产量(图1:A-2,B-2和C-2)。此外,富集的N-1种子培养基通过在N-1阶段支持较长的培养时间而获得较高的最终VCD(图2A,C,E),随后足以支持N阶段生产步骤所需的较高接种密度(图3和4)。因此,富集的培养基既有利于非灌流N-1种子获得更高的最终VCD,也有利于强化Fed-batch生产步骤,获得更高的最终产量或更短的生产时间。
非灌流和灌流培养的N-1种子,其最终的VCD比传统的N-1种子高得多,可以用较小的N-1生物反应器接种较大的N阶段生产型生物反应器,以达到相同的接种密度,从而缩短种子培养时间。使用富集的Batch种子来取代传统的N-1种子,可以为传统的5000L生物反应器生产省去至少一个种子生物反应器步骤。
非灌流式N-1种子培养策略优点是:(1)易于细胞培养过程的开发和操作;(2)不需要专门的灌流设备,也不需要准备和储存大量的灌流培养基;(3)在大多数大规模的商业生产设施中易于实现。
与传统的Batch工艺相比,用非灌流种子接种的强化Fed-batch工艺取得了更高的VCD曲线(数据未显示),这表明收获时宿主细胞蛋白(HCP)可能更高。由于无论接种量大小,在纯化前的HCP值都非常高,所以收获时未测量HCP。尽管如此,这3种mAbs和其他许多蛋白质在最终配制的药物中的HCP水平是相似的。这表明下游工艺足以去除细胞培养物中产生的HCP,而不受不同接种细胞密度的影响。
(虽然本研究中只使用了由CHO细胞培养物生产的3种稳定的mAbs,但非灌流式N-1种子策略的基本原则是缩短种子培养和生产培养时间或提高titer,应该适用于在任何规模的生物制品设施中由不同的哺乳动物细胞和其他宿主生产的其他蛋白质。)
参考文献:
Andrew Yongky, Jianlin Xu, Jun Tian, Christopher Oliveira, Jia Zhao, Kevin McFarland, Michael C. Borys & Zheng Jian Li (2019) Process intensification in fed- batch production bioreactors using non-perfusion seed cultures, mAbs, 11:8, 1502-1514, DOI: 10.1080/19420862.2019.1652075

1、拥有先进的培养基平台、Fed-batch工艺开发平台、灌流工艺开发平台,工艺平台在行业内具有显著的领先优势,可高效提高抗体的产量并优化质量
2、强大的Knowhow能力,自主开发的Maxexpression系列培养基已用于上市项目1项, 超过10项目进入临床阶段,表达量>5g/L。Maxexpression系列培养基平台是与时俱进的平台,始终保持行业先进性,为客户提供快速、低成本、高产量、高质量的项目开发服务
3、商业培养基研究应用作为重点之一,并建立先进商业培养基库,为客户提供高质量而灵活的选择







